雙特異性抗體 (bsAbs) 是一類工程binder,旨在同時靶向兩個化學上不同的表位。這種獨特的結合模式可用于誘導以前無法實現的作用機制,在腫瘤學、自身免疫性疾病、慢性炎癥性疾病、出血性疾病甚至傳染病的許多治療應用方面具有巨大潛力。bsAbs 的結合特性對其功能至關重要,因為形成相互作用的傾向、相互作用的穩定性(半衰期)和平衡親和力都會影響作用機制。對于兩個分子之間的二元相互作用,結合可以用三個生物物理參數直接描述,即結合速率常數 kon、解離速率常數Koff以及平衡解離常數 Kd。對于雙特異性binder,情況更為復雜,因為必須考慮兩種不同的二元相互作用,從而產生三元相互作用(圖 1)。此外,三元復合物可能會因其他協同因素而穩定或不穩定,例如三種結合劑的空間排列、構象靈活性或參與相互作用的分子部分的局部濃度。
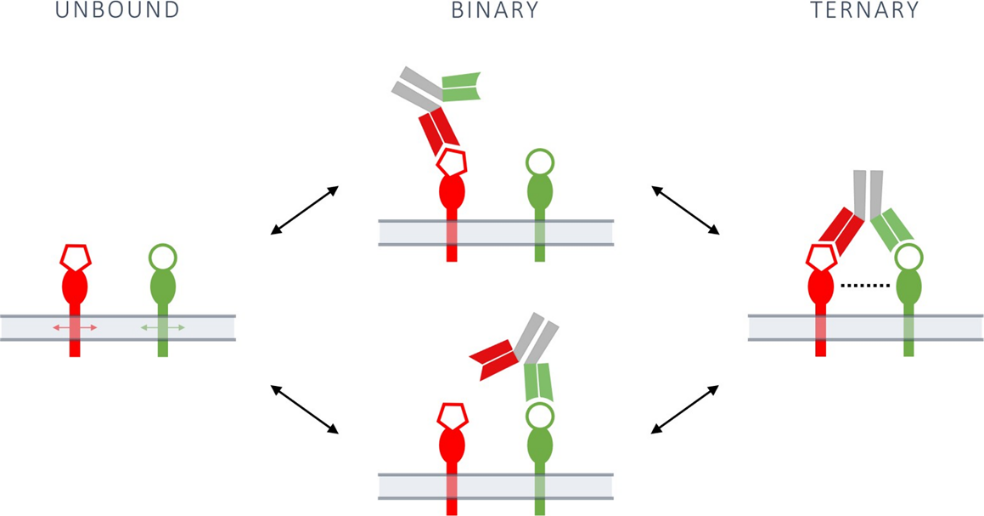
圖1. 雙特異性抗體與細胞表面兩個靶標相互作用的二元和三元結合模式。
三元復合物的穩定性取決于所有可能的(不)結合情況的結合和解離動力學。由于多個參數相互依賴,單獨測量二元結合動力學不足以預測三元復合物的行為。傳統的分子互作分析方法并不適用于表征涉及 bsAbs 的三元復合物。例如SPR)測量得出的結合值與 ELISA 測定和生物活性存在顯著偏差。這可能是因為 SPR 或類似的傳感器無法區分 bsAb 是否與傳感器表面的一個或兩個目標結合,因為折射率傳感只能檢測到傳感器上分析物分子的存在,但無法識別相互作用過程中建立了多少個鍵。此外,當在葡聚糖修飾表面使用常規共價固定策略時,很難以明確的化學計量將一種以上的抗原固定在表面上。最關鍵的限制是此類夾心法檢測不能反映兩種抗原同時在同一細胞表面呈遞給 bsAb 的情況,這會導致抗體結合行為產生avidity。以 emicizumab(商品名Hemlibra®) 為例,avidity實際上是 FX 激活過程中天然血小板表面所需的結合模式,是產生生物活性的先決條件(圖2)。
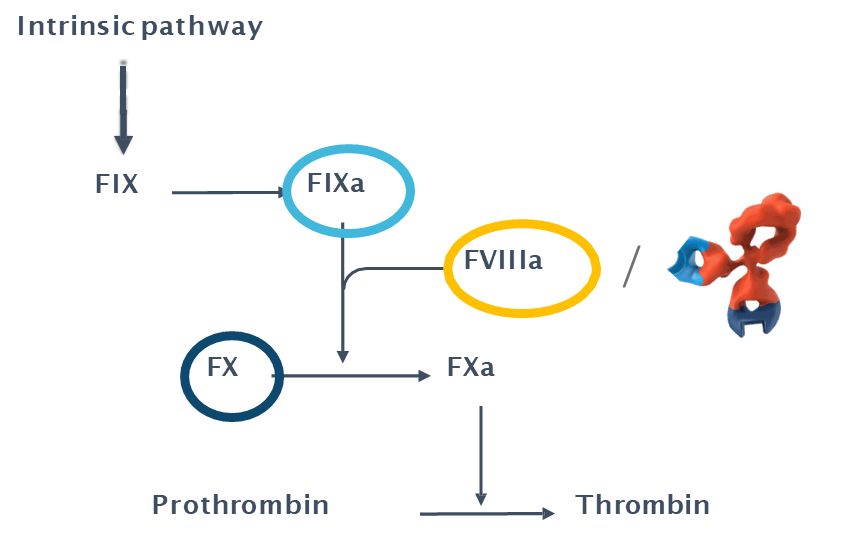
圖2. FIX、FX與FVIIIa形成三元復合物催化凝血酶形成示意圖。
為了描述雙特異性治療性抗體 emicizumab 的二元和三元結合特性。我們設計(見圖3)并使用了一種靈活的Y形DNA納米結構將抗原固定在傳感器上,使兩個靶標都可被溶質bsAb結合。使用雙色熒光檢測,我們可以實時跟蹤emicizumab 的各個互補位與其各自靶標 FIX 和 FX 的結合情況(圖4)。
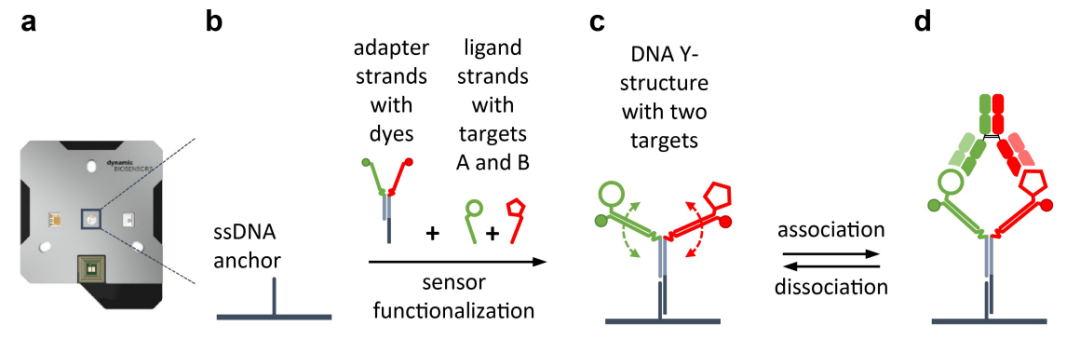
圖3. 芯片及Y結構設計原理示意圖。(a) 帶有微流體通道的 heliX® 生物芯片,該通道具有兩個檢測spot;(b) 單鏈錨定寡脫氧核苷酸共價連接到芯片的金表面,以便進一步與 DNA 功能化;DNA Y 結構由兩條適配鏈組成,這些適配鏈用綠色和紅色染料修飾以進行熒光檢測(實心圓),兩條配體鏈與相應的靶標(FIX = 空心圓,FX = 空心五邊形)結合;預成型的 Y 結構通過將其堿基雜交到芯片表面的“錨”鏈上而固定 (c) 用 DNA Y 結構功能化的芯片表面,具有兩個柔性臂,用于在不同距離處顯示抗原。;(d) Emicizumab 與 FIX 和 FX 靶標結合。測量靠近各個靶標的綠色和紅色染料的熒光變化,以分別分析抗體臂與 FIX 和 FX 的結合。
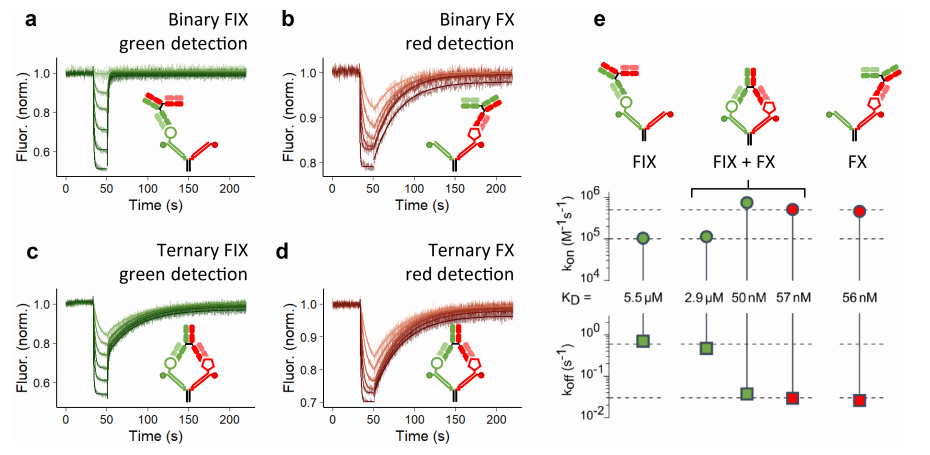
圖4. 實時測量 Emicizumab 與固定在 DNA Y 型結構上的 FIX 和 FX 的結合和解離。bsAb emicizumab 的濃度為 0.0512、0.128、0.32、0.8、2、5 μM。(a) 二元 FIX – emicizumab 相互作用在僅用 FIX(無 FX)修飾的 Y 型結構上測量,信號檢測為綠色。(b) 二元 FX – Emicizumab 相互作用在僅用 FX(無 FIX)修飾的 Y 型結構上測量,信號檢測為紅色。(c) 和 (d) 三元相互作用在用 FIX 和 FX 修飾的 Y 型結構上測量。信號同時以綠色 (C) 和紅色 (D) 測量。(e) 分析的結合(頂部)和解離(底部)速率常數的速率尺度圖,以及解離常數 KD(中間)。二元相互作用 (a、b) 和三元 FX 相互作用 (D) 用單指數擬合函數分析,FIX 臂上的三元相互作用 (C) 用雙指數擬合函數分析。擬合線在測量數據上繪制為平滑線,采樣時間為 200ms。
對 bsAb emicizumab 的二元和三元結合動力學的測量產生了三個重要發現。首先,bsAb 與其兩個靶標的兩種二元相互作用明顯不同,emicizumab 與 FX 的結合速度比 FIX 快 5 倍、穩定 20 倍,總體上強 100 倍。其次,三元結合明顯不同于二元結合,并表現出雙相解離特性。第三,三元結合的發生程度取決于結合階段 bsAb 的濃度。這些結果表明了以下解釋,該解釋以圖形方式總結在圖 5 中。如圖 5(a) 所示,三元復合物的形成發生在低 bsAb 濃度下。在第一步中,當 emicizumab 遇到 Y 結構呈現的兩個靶標時,它最好先與 FX 結合,因為結合速率比 FIX 高 5 倍。在第二步中,emicizumab 的另一條臂與 FIX 結合,后者通過 Y 型結構呈現在 emicizumab 的觸及范圍內。由于 FX 結合的 emicizumab 已經接近 FIX,因此這種交接發生得很快(與 FX 結合相比),這就是為什么在 FIX 的綠色信號中也觀察到了類似 FX 的結合率。當然,emicizumab 與 FIX 或 FX 之間發生二元相互作用而不形成三元復合物也是可能的,也可能通過較弱的相互作用 FIX 捕獲形成三元復合物,但這些過程發生的可能性要小得多。隨后三元復合物開始衰變。一旦兩個靶標都參與其中,三元和二元狀態之間就會發生動態轉變。然而,由于 FIX 的結合力要弱得多,在整個復合物最終完全解離之前,很可能是 FIX 而不是 FX 被其 Fab 釋放并反彈了好幾次或很多次。因此,雖然涉及較弱結合劑 FIX 的相互作用會因強結合劑 FX 的存在而增強,但 FX 相互作用卻幾乎不受弱相互作用劑 FIX 存在的影響,因為它太弱,無法顯著改變 FX 的動力學。因此,在二元和三元情況下觀察到的 FX 動力學相似。
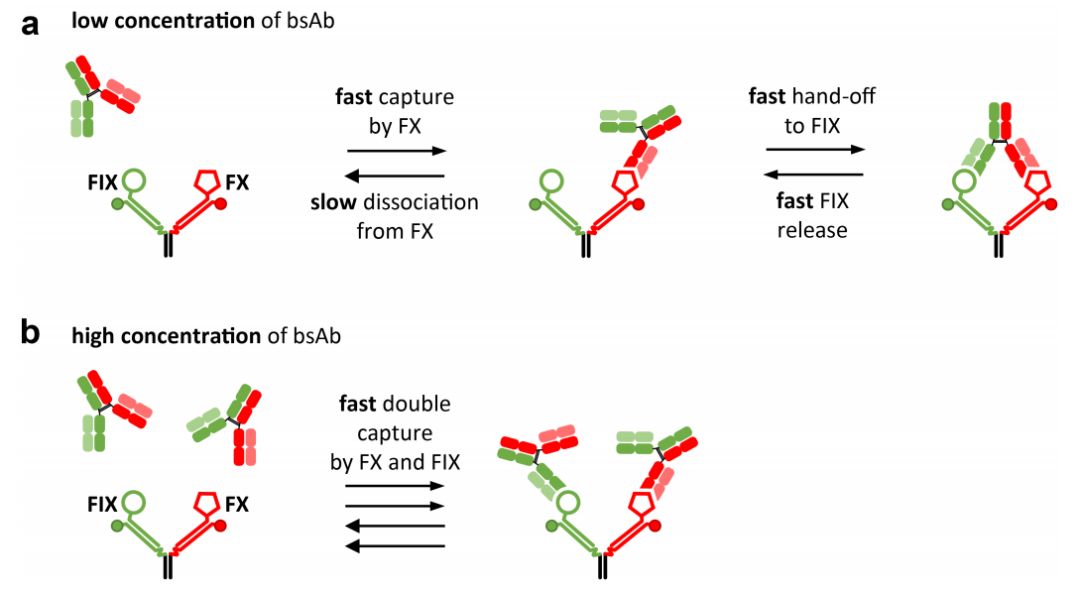
圖 5. 低 (a) 和高 (b) 濃度的 emicizumab 的主要結合模式示意圖。 (A) 在低濃度下,與 FX 的更快結合會捕獲抗體并允許快速移交給 FIX,從而形成三元復合物。(B) 在高濃度下,親和力較低的 FIX 也會快速結合抗體,從而在一個 Y 型結構上產生兩個二元相互作用。(A) 和 (B) 的組合可觀察為濃度依賴性雙指數解離曲線。
如圖 5(b) 所示,在高 bsAb 濃度下,三元復合物的形成受到抑制。在微摩爾濃度的 bsAb 下,溶液中的 bsAb 結合與 FX 促進的捕獲和交接機制競爭。預計當溶液中的抗 FIX Fabs 濃度超過 Y 結構上的局部濃度時會發生這種情況,該濃度已確定在 0.1–0.2 μM 范圍內。因此,當溶液中的 bsAb 濃度遠高于 0.1 μM 時,二元結合模式下的雙重捕獲更受青睞。在較高分析物濃度下形成的三元復合物較少,這一發現讓人想起高劑量“hook”效應,這是免疫測定中的常見干擾。通常,在結合過程中,抗體的一條臂與一個靶標結合,然后第二條臂與第二個靶標結合,形成三元復合物。在高分析物濃度下,兩種抗體同時與一個靶標對結合的可能性更大,從而阻止三元復合物的形成。了解這些結合特性使我們能夠了解 emicizumab 在體內的作用方式。在血漿中,FIX 和 FX 的濃度分別為 90 和 135 nM。盡管預計 Emicizumab 會與溶液中的兩種凝血因子頻繁相互作用,但模擬表明,只有極小部分的 Emicizumab 在血漿中形成三元復合物。這是因為,如果其相互作用沒有通過 FX 介導的表面親和力穩定,它會快速與 FIX 解離。只有當 FIX 和 FX 在損傷后與活化的血小板結合時,才能與 Emicizumab 建立三元復合物。

heliX+分子互作分析系統采用switchSENSE®技術,通過共價偶聯或標簽捕獲方式將感興趣的分 子(配體)固定在heliX®芯片上,結合標準的自動化 工作流程為分子互作提供高效解決方案。
同騰睿杰(上海)生物科技有限公司作為Dynamic Biosensors中國總代理商,為您提供優質的售前售后服務。
聯系電話:021-50826962
聯系郵箱:sales@ttbiotech.com




