在生物學,便攜式DNA測序,無標記單分子分析和納米醫學方面,膜納米孔都體現了其重要的應用價值。傳統的物質運輸,其依賴于膜上數納米寬的桶狀通道,但是科技發展的需求,需要在形狀上可調控的,更加寬的納米通道,以適應更廣泛的應用。而在天然狀態下,并不存在這種類的納米孔。利用蛋白合成該類型的納米通道,也具有極大的挑戰性。本文介紹了利用DNA進行上述結構可調和功能應用多樣化的膜納米孔的設計。該設計將成束的DNA雙鏈制備成構成膜孔的亞單位,并逐步組裝成形狀上可調節的完整性膜孔,該孔的寬度可達幾十納米。用于識別或信號連接的功能單位,可以與該納米孔進行結合。通過現有儀器設備和檢測手段,本文證明了該定制化的納米孔在電介導的10nm大小的單分子蛋白的檢測上應用潛能,并顯示了在合成生物學,單分子酶學和生物物理分析以及便攜式診斷,環境檢測等方面,該DNA納米結構如何實現對功能性分子的傳遞作用。
膜納米孔的的腔面性質或參數決定了其生物學功能。在納米孔對物質的感應中,通道的寬度調控著單個分子的進入及通過的過程,并因此影響了由于物質通過引起的電信號。因此,1-5nm寬度的蛋白孔通道能夠感應相同大小的DNA鏈,有機分子和小分子量蛋白。而克服當前由于通道寬度帶來的限制,是膜納米孔研究領域的重大突破。例如,更寬的納米孔能夠在單分子水平上,更快轉移,直接的感應及檢測分子量更大的酶,免疫球蛋白,蛋白復合物或病毒。并且,在形狀上,突破傳統的圓柱形通道設計,能夠更好的應用于不同形狀的底物。并且,該納米孔應能夠連接特異性的分子受體,提高分子識別和結合的特異性。最后,該二代納米孔,應能夠和當前的電信號檢測設備兼容,比如用于便攜式DNA測序的MinlON,目前為止,該技術還未應用于蛋白分子的檢測中。除了分子感應,納米孔還可以應用于合成的細胞,細胞打孔以用于生物活性物質的轉運。目前為止,由于氨基酸較小以及多肽折疊成特定蛋白結構的復雜性,還未有蛋白,肽等構建的符合需求的二代膜納米孔。由于核酸分子具有簡單的堿基互補配對法則和較容易預測的DNA折疊性質,DNA成為了構建該二代納米孔的可替代材料。確實,已有報道,DNA能夠制備成直徑達10nm的納米通道。所有已有的DNA納米孔均采用DNA雙鏈平行排列的形式插入膜中。
在該文獻中,深入詳細的闡述了DNA分子如何突破當前的技術限制,增加了納米孔的尺寸及增加了孔形狀的多樣性。在最初的DNA納米孔設計中,我們受限于所有DNA雙鏈需以直角的方式插入膜中的要求。為了克服這種限制,我們利用DNA搭建的方式,將DNA雙鏈成束搭建成納米孔模塊,插入膜中,并組裝成完整的納米孔,請見Fig. 1a-c。模塊化的應用能夠提高大小和形狀上的靈活性,比如可以構建成三角形,方形,五邊形和六邊形。請見Fig. 1d。結合可調控的邊長(10和20nm)的亞單位,構建的納米孔腔面積可從43nm2到400nm2,請見Fig. 1d。相比于傳統的蛋白構成的納米孔,大小提高了260倍。
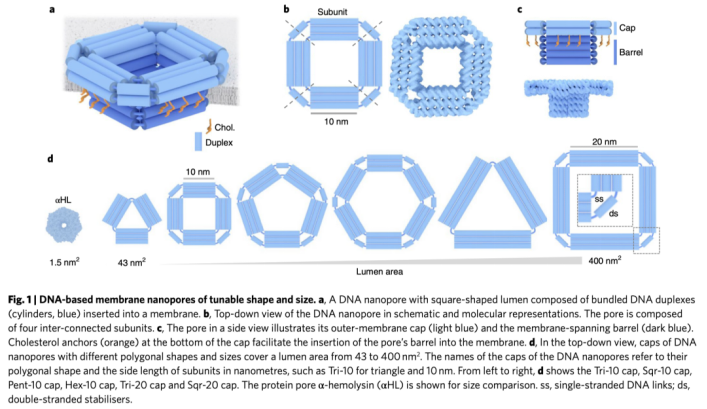
可調控大小和形狀的DNA膜納米孔示意圖
我們設計的納米孔,帶有一個額外的帽結構,該結構決定了整個孔的形狀,即帽下插入膜中的桶狀結構。同時,該結構還具有以下特性:該帽狀結構可通過雙鏈亞單位的數量,調節其高度和寬度;該帽狀結構內部,可通過短的單鏈或雙鏈DNA進行連接;此外,穩定的內部DNA雙鏈可以防止帽的不穩定及形狀的變化;在自我穩定的三角形中,內部可以不需要DNA雙鏈連接;確定的帽的幾何形狀定性了孔的跨膜形狀。在我們目前的設計中,膜孔壁由一個雙鏈厚度組成,但更厚的孔壁是完全可以實現的。在膽固醇脂質的作用下,桶狀結構插入膜中。該孔狀的設計不僅使得該孔插入到脂質雙分子層中,并且可以插入到MinlON flow細胞膜中,以用于免疫學相關的蛋白檢測。
我們首先設計一系列六邊形帽,不帶有穿膜的桶狀結構,用以檢驗膜孔的設計。包括10nm亞單位構成的三角形-10nm帽,方形-10nm帽,五邊形-10nm帽,六邊形-10nm帽;20nm亞單位構成的三角形-20nm帽和方形-20nm帽。請見Fig. 1d和2a。組裝路徑包括混合DNA骨架的程序性折疊和DNA寡核苷酸鏈退火形成特定的納米結構。經此產生的自組裝DNA帽成分均一,可經DNA凝膠電泳進行驗證是否為均一的單條帶。請見Fig. 2a。
帽結構可經凝膠電泳并純化后,由負染以及電鏡進一步確定其結構。與設計的方案一致,帽的結構呈現預期的多邊形形狀以及亞單位長度,如長度分別是9.62 ± 0.69 nm, 9.86 ± 0.37 nm 和20.17 ± 1.74 nm的三角形-10nm帽,方形-10nm帽和方形-20nm帽。
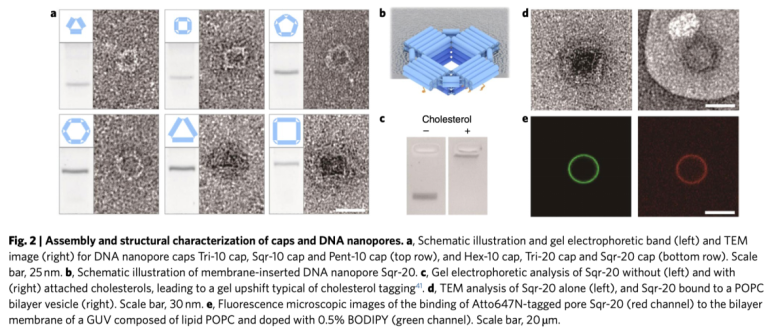
DNA納米孔帽結構及孔結構的組裝和性質鑒定
在確定帽設計的可行性后,我們測試了帶有桶狀的穿膜的納米孔通道是否可以在形狀和大小上進行調節。我們測試了三角形-10nm, 方形-10nm和方形-20nm。請見Fig. 2b。對于該結構和膜的相互作用方面,在5x2的雙鏈DNA帽下方攜帶了幾個固醇類生物標簽,每個10nm亞單位連接10個標簽,每個20nm亞單位連接15個標簽。第一步,首先組裝不帶有標簽的孔狀結構,自裝后產生與預期一致的單條帶的DNA以及與預期一致的電鏡結構。第二步,膜孔上連接固醇類標簽。可通過凝膠電泳條帶大小判斷標簽連接的結果。請見Fig. 2c。
為了驗證固醇類標簽能夠促進納米孔和脂質膜的結合,通過電鏡直接對標有固醇的方形-20nm的納米孔在小的膜泡上的形狀進行結構分析。并用Atto647N-標記的方形-20nm納米孔和膜的脂質POPC的熒光共定位進一步確認其與膜的結合。請見Fig. 2e。
可通過單通道電流檢測的方法,確認DNA納米孔以確定的,可調控的通道腔的方式插入脂雙分子層。當電壓施加于膜上時,該技術可記錄通過通道的電子流。我們分析了三角形-10nm納米孔,方形-10nm納米孔和方形-20nm孔的電子流,其電導率隨著納米孔的大小增加而增加。請見Fig. 3a, b, c. 在1 M KCl, 10 mM HEPES, pH 7.4和+50 mV的跨膜電勢的標準條件下,納米孔的電流未出現變化。此外,更大的納米孔產生了更高的電導率,平均變化如下:2.10 ± 0.21 nS (n = 19), 4.58 ± 0.27 nS (n = 29) 和8.91 ± 0.33 nS (n = 17; Fig. 3a(iv),b(iv),c(iv))。三角形-10nm的納米孔與方形-10nm的納米孔之間電導率的檢測值差異是2.2倍,和理論預期的1.8倍差異幾乎一致。方形-10nm和方形-20nm納米孔之間的電導率檢測值差異是1.9倍,比預期值2.8倍低。可能是因為來自側面膜的壓力可能影響了插入其中的通道的大小,可通過增加通道的穩定性而減少這種差異。
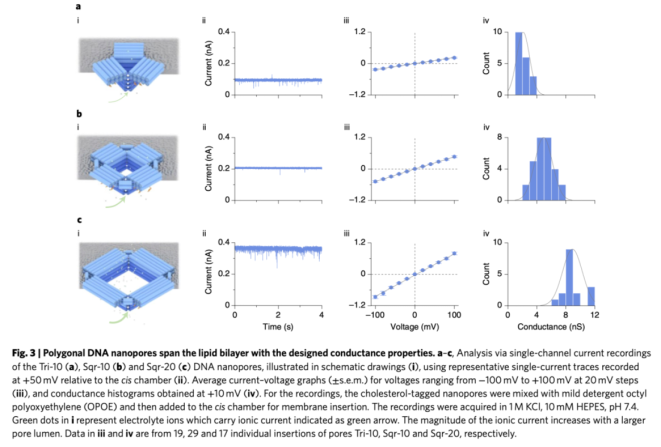
多邊形DNA納米孔的電導性能檢測
DNA膜納米孔對IgG蛋白分子
的轉運及檢測性能鑒定
我們進一步測試了DNA納米孔在單分子水平上對無標記的,特異性的IgG抗體進行檢測的能力。我們選擇方形-10nm的納米孔,以適配10nm大小的IgG分子。納米孔連接有生物素標簽,用于特異性結合抗生物素抗體。斑點印跡法確認了抗體與生物素標簽的特異性結合。在單通道電流記錄檢測中,標簽并未對電導特性產生影響,請見Fig. 4b,然而抗體的添加導致了電流的阻塞,說明存在單個結合事件的發生,請見Fig. 4b。而此單個事件發生的頻率和抗體濃度具有良好的線性相關性,可以通過抗體濃度和1/τon的線性關系進行說明,τon代表的是事件發生的間隔時間,請見Fig. 4b。同時,我們由非生物素化的方形-10nm的對照納米孔以及非特異性抗體對照組可知,上述結合是特異性的。同樣,非同源性BSA做為底物時,生物素化的方形-10nm納米孔未出現電流阻塞效應。
抗體結合的單分子動力學效應可通過納米孔的電流相對幅度A/I o變化,請見Fig. 4b以及持續時間,τ off 變化進行檢測,請見Fig. 4b。并對它們之間相對關系進行分析,請見Fig. 4d。超過95%的結合事件的電流幅度在48.2 ± 7.7% (±s.d., n = 205; Fig. 4d) 。平均的持續時間τoff在0.66 ± 0.02 s。參數τoff 和 τon 分別代表動力學解離和結合常數Koff和Kon,請見Fig. 4c。抗體的解離常數和結合常數分別是1.79 ± 0.05 s ?1 和1.89 ± 0.38 × 10 9 M ?1 s?1。經由該納米孔測量得到的參數稍高于經由switchSENSE技術測量值0.056 ± 0.001 s?1 和1.73 ± 0.05 × 10 8 M ?1 s ?1 。
單分子平衡解離常數Kd=Koff/Kon, 在該納米孔體系下測量值為9.45 ± 1.92 × 10 ?10 M (±s.e.m.),接近于switchSENSE技術測量值3.25 ± 0.11 × 10 ?10 M。說明了經由納米孔進行分子結合分析的合理性。依賴于電壓的電信號記錄說明蛋白通過電泳的方式通過納米孔,而非通過電滲透。僅正電勢可以導致抗體結合的電流阻塞和產生由抗體運動引起的更高的能量譜也可以證明這一點,請見Fig. 4e和Fig. 4f。BSA通過非生物素化的DNA納米孔的過程中,也可以檢測到該電泳現象。
最后,我們評估了DNA納米孔是否可以插入MinION flow 細胞中,并靈敏的感應人SARS-CoV-2抗體。為了更好的與Y型結構的抗體適配,可以選擇三角形-20nm的膜納米孔。請見Fig. 4g。
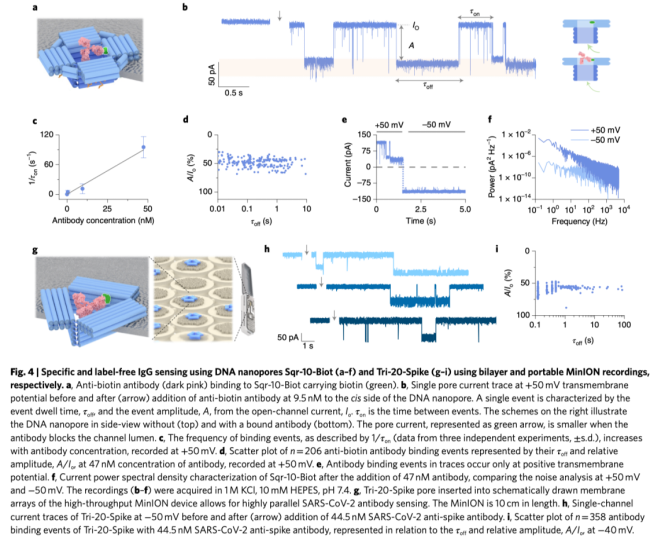
DNA納米孔對特異性無標記IgG分子的檢測作用
當抗體的受體沒有與納米孔連接時,三角形-20nm納米孔能夠產生穩定的單通道電流,其平均電導率為7.83 ± 0.71 nS (±s.e.m., n = 9),高出對照的方形-10nm納米孔1.7倍,與預期的電導率差異一致。三角形-20nm的納米孔與SARS-CoV-2 刺突蛋白連接后,成為特異性識別SARS-CoV-2抗體的納米感受器。請見Fig. 4g。刺突蛋白與納米孔腔的結合是通過不可逆轉的金屬螯合作用,將分子連接到寡聚核苷酸上。帶有刺突蛋白的DNA納米孔,可以產生穩定的電流輸出,平均電導率為1.8 ± 0.2 nS (±s.e.m., n = 23) ,低于未連接刺突蛋白的三角形-20nm納米孔的電導率。
當加入人的 SARS-CoV-2 抗體后,能夠產生納米孔的電流阻塞效應,請見Fig. 4h,說明抗體與孔內受體發生結合效應。結合效應產生的相對電信號幅值為61.7 ± 6.9% (±STD, n = 357) ,平均結合時間為1.7 ± 8.6 s (±STD, n = 357; Fig. 4i)。該數據表明,三角形的納米孔形狀能夠導致更高的電流阻塞。
膜納米孔在科學研究中已經顯示出重要的價值,我們的研究集中于開發在大小和形狀上能夠更加靈活調控的納米孔。該研究依賴于DNA納米技術得以實現。通過目前的常見檢測設備,我們通過單分子蛋白通過納米孔時的參數證實了該膜納米孔的應用價值。對于傳統的以蛋白質為材料構建的納米孔,由于孔徑的限制,無法對10nm大小的底物進行檢測。而分子直接進入納米腔中,能夠最大的獲取單分子的生物物理性質,酶活性或相互作用特性等方面的信息。根據底物的大小對納米孔進行定制,可以實現納米孔和底物的最佳匹配。更大的納米孔可以用于不規則的幾何構建,匹配非對稱性的底物分子。總體上看,該人工合成的納米孔,突破了在天然狀態下的膜孔無法實現的功能,幫助轉運并快速方便的檢測與其相互作用的蛋白分子,顯示出重要的市場應用價值。




