在生物醫學領域,藥物研發始終是一場與時間賽跑、與病魔較量的艱苦征程。近年來,新藥研發的步伐逐漸放緩,從1991-2000年21個主要國家發現367種新藥,到2001-2010年降至251種,進入臨床試驗的新藥數量也越來越少,研發周期越來越長[1,2]。這背后的原因復雜多樣,其中藥物研發過程中化學合成與生物篩選環節的分離和不兼容,成為了阻礙新藥研發的關鍵因素。傳統的有機合成方法不僅耗時耗力,且合成過程中大量使用的有機溶劑和嚴苛條件,與生物篩選所需的溫和水性環境及小型化、平行化要求格格不入。不過,一項名為chemBIOS的創新技術平臺的出現,為這一困境帶來了轉機。
chemBIOS平臺與合成所需的有機溶劑和生物篩選所需的水溶液相容。我們使用chemBIOS平臺進行75個平行的三組分反應來合成一個脂質體庫,然后通過MALDI-MS進行表征,在芯片上形成lipoplexes,并在芯片上進行細胞篩選。從文庫合成到細胞篩選的整個過程僅需3天,總溶液量約為1mL,證明了chemBIOS技術在提高效率、加速篩選和藥物開發方面的潛力。
LSTL玻片:通過硅烷化處理和光化學硫醇-烯點擊反應,在玻璃表面形成親疏兩性圖案(圖1a)。親水性區域可穩定低表面張力有機溶劑(如DMSO),疏水性邊界則通過全氟癸硫醇(PFDT)修飾,實現微滴陣列的精準控制。
HSTL玻片:涂覆多孔聚(甲基丙烯酸羥乙酯-共-二甲基丙烯酸乙二醇酯)聚合物層,結合光化學硫醇-炔點擊反應,形成親水性斑點(接觸角<10°)與超疏水性邊界(接觸角>150°),適用于高表面張力水溶液(如水、脂質體)的微滴陣列(圖1b)。
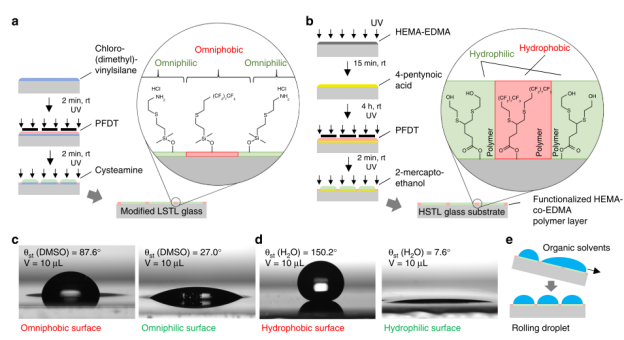
圖1. 用于chemBIOS平臺的圖案化載玻片的制造和表征。chemBIOS平臺由兩種類型的圖案化載玻片組成。a.與低表面張力液體相容的載玻片(LSTL載玻片)是通過使用氯(二甲基)乙烯基硅烷對玻璃表面進行硅烷化,并通過光化學硫醇-烯點擊反應形成圖案而制備的。通過與全氟癸硫醇(PFDT)反應生成全疏邊界,然后通過半胱胺鹽酸鹽形成全嗜斑點。斑點直徑2.83mm;疏水邊界寬度1.67mm。b.用于高表面張力液體的載玻片(HSTL載玻片)通過聚合反應來制造,以施加聚(2-羥乙基甲基丙烯酸酯-共-乙烯二甲基丙烯酸酯)的多孔聚合物層。用4-戊炔酸的官能化使得能夠通過硫醇炔光點擊化學進一步形成表面圖案。通過PFDT生成疏水邊界,然后使用2-巰基乙醇形成親水斑點。斑點直徑2.83mm;疏水邊界寬度1.67mm。c. DMSO液滴在用于具有相應靜態接觸角的LSTL圖案的全疏表面和全親水表面上的照片。液滴體積:10 μL。d. 用于HSTL載玻片的疏水和親水表面上水滴的照片,具有相應的靜態接觸角。液滴體積:10 μL。e. 示意圖顯示了圖案化LSTL載玻片上的不連續去濕效果,這使得能夠手動生成有機液滴陣列
I.DOT精準分配:利用I.DOT非接觸式移液系統(死體積 <1 μL),將胺類溶液(A1-A5)與硫代內酯/吡啶基二硫化物混合物分別以列、行方式精準分配至LSTL玻片(圖2a)。75個微反應器同步反應2小時,產率達89±15%。
產物表征:通過MALDI-TOF質譜(圖2c)驗證結構,片上液-液萃取技術(圖3)分離親水/疏水染料(亞甲藍純度91%,尼羅紅57%)。

圖2. 一個脂質體庫的片上合成和表征。a. 使用chemBIOS平臺組合合成脂質體的示意圖。在第一步中,將溶解在DMSO中的各種胺逐柱施加到低表面張力液體(LSTL)載玻片A上。然后,將溶于DMSO的硫內酯和吡啶基二硫化物衍生物的混合物以與載玻片A上的列正交的行施加到LSTL載玻片B上。通過滾動溶液液滴以形成成排的單獨液滴來進行施加。在下一步驟中,將載玻片A和載玻片B彼此夾在中間(SW)以使各個液滴接觸以合并液滴,從而引發反應。在室溫下2小時后完成反應。在單個載玻片上一式三份合成每個載玻片25種不同的脂質體。b. 反應方案和反應的所有不同前體的列表。c. 為了表征所產生的化合物,將載玻片A夾在MALDI板上,然后加入基質并干燥板。MALDI-TOF質譜測量(插圖中所示的光譜實例,正模式)使得能夠快速且方便地表征合成化合物的整個庫。(i)靜置,然后加入含有0.1%v/v三氟乙酸的1:1乙腈:水的10 mg·mL?1 α-氰基-4-羥基肉桂酸溶液。源數據作為源數據文件提供。
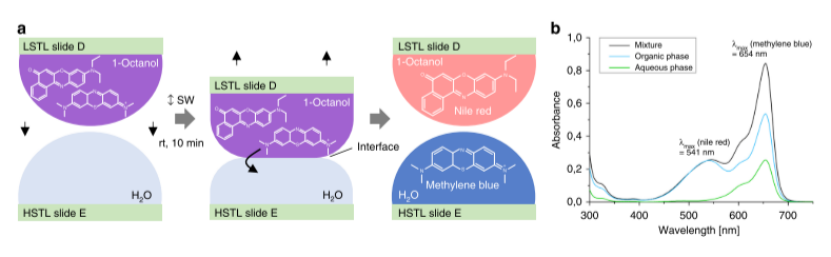
圖3. 片上平行液-液萃取。a芯片上兩相液體萃取過程的示意圖。親油尼羅紅和親水性亞甲基藍在1-辛醇的LSTL載玻片D上的混合物,通過將載玻片與HSTL載玻片E進行10分鐘的水滴分離。兩種不混溶的溶劑之間形成界面,并將水溶性亞甲基藍提取到水相中。B通過紫外-可見光譜法驗證芯片上提取。混合物的UV-Vis光譜顯示兩個局部吸收最大值:一個在541 nm處對應于尼羅紅,另一個在654 nm處對應于亞甲基藍。萃取后,有機相中亞甲基藍的最大吸收強度降低,而尼羅紅的最大吸收強度保持不變。在水相中,沒有檢測到尼羅紅。源數據作為源數據文件提供。
自動化轉移:I.DOT將干燥的脂質體轉移至HSTL玻片(圖4a),與含質粒DNA(pCS2-GFP)的醋酸鈉緩沖液共孵育,形成脂質復合物(lipoplexes)。動態光散射顯示,lipoplexes粒徑(515±34 nm)顯著大于脂質體(376±122 nm),zeta電位更低(-16mVvs+27mV,圖4b)
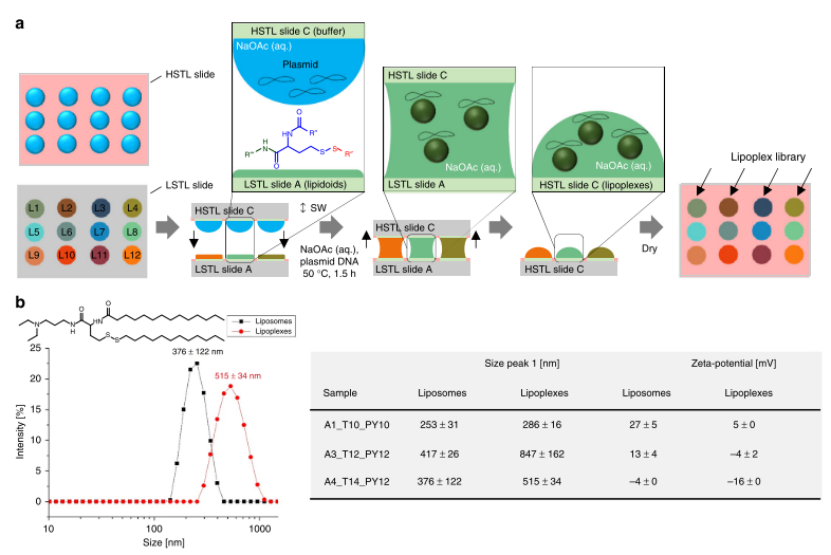
圖4. 脂質體或脂質復合物文庫的芯片上平行形成。a脂質復合物形成的示意圖。將含有蔗糖、明膠、纖連蛋白和pDNA(pCS2-GFP)的水性乙酸鈉緩沖液滴的陣列(HSTL載玻片C)與含有干燥的脂質體文庫的LSTL載玻片A夾在一起,然后在50°C下孵育1.5小時并干燥,然后將載玻片C用于以下反向細胞轉染實驗。以相同的方式產生脂質體,而不添加質粒DNA。B脂質復合物和相應脂質體的動態光散射(DLS)和ζ電位分析的結果。脂質體顯示出比相應的脂質復合物更小的顆粒和更高的ζ電位。?值為標準偏差,n=3(重復次數)。源數據作為源數據文件提供
細胞打印與分析:通過I.DOT將HEK293T細胞懸液(6×10?cells/mL)精準打印至lipoplexes陣列(圖5a),48小時后通過Hoechst/PI染色和熒光顯微鏡分析轉染效率。最優脂質體A3_T14_PY14實現52±4%轉染效率(圖5b),優于商業化試劑ScreenFect A(34%)。

圖5. 所產生的lipoplex文庫的芯片上反向細胞轉染篩選。a顯示芯片上細胞轉染篩選過程的示意圖。將5微升的HEK 293 T細胞懸浮液印刷到HSTL載玻片C上的每個親水性斑點中,所述HSTL載玻片C被干燥的lipoplex細胞轉染混合物覆蓋。在36 °C和5%C02下孵育陣列48小時后,將1 μL染色溶液打印到每個液滴中,然后孵育15分鐘并進行熒光顯微鏡分析。B可視化轉染效率(GFP轉染細胞數/總細胞數)平均值的條形圖,其基于覆蓋整個管道的三個獨立實驗(重疊的點圖)計算,包括芯片上文庫合成、脂質復合物的形成和細胞轉染。在我們的研究中,A3_T14_PY14脂質體被證明是最有效的,導致52 ± 4%的轉染效率。誤差條是標準偏差,n=3(重復次數); N=3(重復次數,包括脂質合成)。源數據以源數據文件的形式提供。c pCS 2-GFP轉染細胞的熒光顯微鏡圖像。比例尺:200 μm
chemBIOS平臺通過“芯片級化學-生物聯姻”首次實現了溶液相有機合成與高通量生物篩選的無縫銜接,其核心驅動力I.DOT非接觸式移液技術具備三大優勢:一是精準操控,通過納升級液體分配確保反應一致性并降低交叉污染風險;二是高通量整合,支持多步自動化操作(如細胞打印、試劑添加)以加速藥物篩選流程;三是兼容性擴展,未來可結合I.DOT的液滴融合技術(如proMAD方法)構建更復雜的3D細胞模型(如腫瘤球體),進一步拓展個性化醫療應用潛力。
盡管chemBIOS展現了巨大潛力,但高溫反應、固相試劑添加及高通量純化仍是待解決的難題。通過I.DOT的智能化升級(如動態液滴監測),可進一步提升平臺的靈活性與普適性。未來,結合微流控技術與自動化系統,該平臺有望推動“按需合成-實時篩選”的精準藥物研發模式,為個性化醫療和罕見病藥物開發提供革命性工具。

同騰睿杰(上海)生物技有限公司作為CYTENA I.DOT中國總代理商,為您提供優質的售前售后服務。
聯系電話:021-50826962
聯系郵箱:sales@ttbiotech.com




